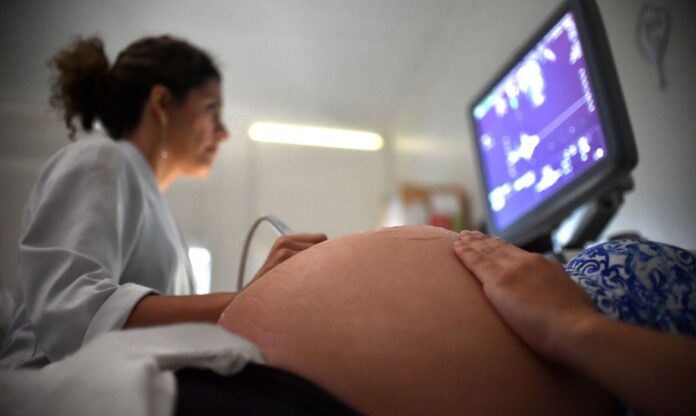
Pesquisadores brasileiros do Instituto de Matemática Pura e Aplicada (Impa) desenvolveram um algoritmo que analisa imagens de ressonância magnética com rapidez e precisão, o que pode ajudar médicos a detectar problemas na gestação.

Esse algoritmo consegue detectar, com taxa de 93% de acerto, o que é o líquido amniótico, substância que envolve o bebê em desenvolvimento. Uma das funções do líquido amniótico é proteger o feto.
A quantidade de líquido amniótico pode interferir no desenvolvimento do feto. Um menor volume de líquido ou uma quantidade em excesso podem trazer dificuldades para a gestação, caso não sejam tratadas adequadamente.
“Ver a normalidade do líquido amniótico é muito importante porque ele reflete, primeiro, o bem estar do feto, e reflete também a possibilidade de algumas patologias”, disse Heron Werner, médico da rede de saúde integrada Dasa e um dos responsáveis pelo estudo.
Segundo ele, se a quantidade de líquido amniótico estiver aumentada, isso pode significar uma patologia gastrointestinal ou uma má formação do sistema nervoso central do feto. Também pode significar que a mãe tem diabetes.
Do contrário, se o volume de líquido estiver diminuído, pode indicar que o bebê é pequeno ou que há uma insuficiência placentária. Também pode significar um problema na função renal. Por isso é importante analisar com precisão a quantidade de líquido amniótico na gestação, diz o médico.
Exame
Atualmente, a maneira como o volume do líquido amniótico é calculado é subjetiva. Quando um exame de ultrassom aponta algum problema para a gestação, os médicos solicitam um novo exame, uma ressonância magnética.
“A ressonância é um exame que a gente usa para ajudar na ultrassonografia quando o feto tem algum problema [identificado] no ultrassom. A vantagem da ressonância é que ela me dá uma visão do conteúdo uterino como um todo, que a ultrassonografia não consegue dar numa imagem só. Com ela consigo ter informação em cortes de todo o volume uterino. Além disso, o líquido amniótico tem um sinal muito aumentado na ressonância, o que o destaca do resto do conteúdo uterino, que seria o feto, placenta e cordão umbilical”, explicou Werner.
Após essa ressonância, o médico então começa a analisar as imagens. “Se eu quisesse um cálculo de precisão, eu teria que pegar todos os cortes da ressonância, desenhar a área do liquido amniótico em cada corte e fazer o cálculo. E isso iria levar horas já que tenho em torno de 200 cortes em uma ressonância”, disse o médico.
“O que acaba acontecendo é que esse médico tem, foto por foto, que delinear o que é líquido amniótico e o que não é. E costuma ser mais de 100 camadas ou fotos. Depois de fazer tudo isso, ele consegue dar uma estimativa de volume. É um calculo somando a área em cada uma das fotos. É um processo demorado”, explicou Paulo Orenstein, pesquisador do Impa e também um dos responsáveis pelo estudo, em entrevista à Agência Brasil.
“Em casos usuais, a maneira como é estimado o líquido amniótico é totalmente no olho. Ele [médico] olha na barriga, vê o tamanho da circunferência e decide se é pouco não. Poucos médicos fazem isso bem. E isso é perigoso justamente pelo fato de que essa quantidade de líquido é indicativa [de patologias]”, disse o pesquisador do Impa.
Inteligência artificial
Com o desenvolvimento dessa inteligência artificial, desse algoritmo, esse processo pode ficar mais rápido e eficiente. Por meio dela, essa estimativa de volume do líquido amniótico pode ser feita em cinco segundos: ou seja, se ela já estivesse plenamente desenvolvida e em operação, uma gestante poderia saber o volume do líquido enquanto estivesse ainda fazendo o exame de ressonância magnética.
Para desenvolver essa inteligência artificial, a Dasa enviou aos pesquisadores do Impa cerca de 700 exames de ressonância magnética, com anotações dos médicos delimitando o que era ou não o líquido amniótico. “O que a gente queria era construir um algoritmo que conseguisse replicar o mesmo nível de acurácia que um médico que teve anos de treinamento tem. Dividimos esses 700 exames em duas classes: uma de treino; outra de testes. Destes 700 [exames], 500 exames foram usados para treinar nosso algoritmo e 200 exames foram usados para testar se o algoritmo estava indo bem ou não”, explicou o pesquisador do Impa.
A parte de treinamento, explicou ele, é semelhante ao processo que ocorre com humanos. “Não é muito diferente de como se treinaria um ser humano. O algoritmo começa de uma maneira quase aleatória, chutando naquela imagem o que é líquido e o que não é. Por exemplo, no caso de uma criança. Você tem que ensinar a ela o que é uma árvore. E as vezes ela olha para um carro e pode dizer que é uma árvore. Você então a corrige e diz: ‘não é uma árvore’. Aos poucos, se você fizer isso várias vezes, ela acaba aprendendo”, comparou.
Depois dessa etapa de treinamento, vem a fase dos testes. “Depois de treinar e do algoritmo ter visto esses 500 exames, pegamos 200 exames que ele nunca viu, exames que ele não decorou, e a gente volta a perguntar a ele o que é ou não liquido amniótico”, disse Orenstein.
Esse processo todo, disse ele, ocorre por tentativas e erros. E durante essa preparação da inteligência artificial para identificar o líquido amniótico, houve um grande erro: o algoritmo apontou como líquido amniótico o que, em verdade, foi analisado por um médico como um cisto. Depois disso, o pesquisador “ensinou” o algoritmo a entender esse novo processo.
Próximos passos
Em entrevista à Agência Brasil, o pesquisador do Impa disse que um dos próximos passos para o desenvolvimento dessa tecnologia é continuar recebendo mais dados para aprimorar a capacidade do algoritmo e poder identificar outros problemas. Hoje, ele está sendo estudado para identificar o volume do líquido amniótico. Mas uma das intenções dos pesquisadores é permitir que ele identifique também, por exemplo, os órgãos do feto.
“Se tivermos um feto cujo cérebro esteja com tamanho menor do que o esperado para aquela idade, nosso algoritmo hoje não identificaria isso. Mas nossa esperança é evoluir nessa direção mais complicada do problema, e tentar dar uma solução mais abrangente para outros tipos de patologia”, disse Orenstein.
Outro passo é permitir que essa solução possa ser utilizada com facilidade pelos médicos. “É claro que se queremos que médicos usem essa solução, a gente precisa melhorar, acoplar esse algoritmo a ferramentas médicas. Basicamente pegar o software que os médicos usam e embutir nosso algoritmo como opção de uso. Por exemplo, colocar nosso algoritmo em uma máquina de ressonância magnética”, explicou o pesquisador.
Para Werner, esse algoritmo poderá permitir que o médico avalie, com mais precisão, a necessidade de intervenções intrauterinas. “Existem intervenções intrauterinas que podem ser feitas e ajudar no bem estar fetal. Em muitos casos, não precisa. Mas ele [o algoritmo] chama a atenção para fazer esse acompanhamento”, disse o médico Werner.
Fonte: Agência Brasil