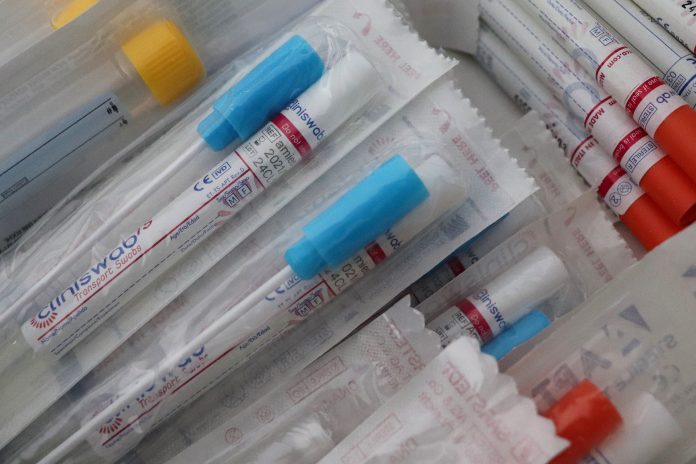
Em 15 de agosto, o órgão americano Food and Drug Administration (FDA) emitiu uma autorização de uso de emergência à Yale School of Public Health para a utilização do teste diagnóstico SalivaDirect COVID-19, um novo tipo de teste para detecção do vírus SARS-CoV-2 na saliva, o que poderia reduzir os custos e o tempo para processar os resultados.
A coleta do teste não requer nenhum tipo especial de cotonete ou tubo: a saliva pode ser recolhida em qualquer recipiente estéril. Este teste também é único porque não requer uma etapa separada de extração de ácido nucleico. Isso é bastante significativo, pois os kits de extração usados para esta etapa em outros testes estavam sujeitos à escassez.
De acordo com a FDA, ser capaz de realizar um teste sem esses kits aumenta a capacidade de aumentar a quantidade de testes, ao mesmo tempo em que reduz a pressão sobre os recursos disponíveis. Além disso, a metodologia SalivaDirect foi validada e autorizada para uso com diferentes combinações de reagentes e instrumentos comumente usados, o que significa que o teste pode ser usado amplamente na maioria dos laboratórios de alta complexidade.
Licença aberta do teste de saliva
A intenção de Yale é fornecer o protocolo SalivaDirect para laboratórios interessados como um protocolo de “código aberto”, o que significa que laboratórios designados podem seguir o protocolo para obter os componentes necessários e realizar o teste em seu laboratório de acordo com as instruções de uso de Yale.
Como esse teste não depende de nenhum equipamento proprietário da Yale e pode usar uma variedade de componentes de teste disponíveis comercialmente, ele pode ser montado e usado em laboratórios de alta complexidade em todos os Estados Unidos, desde que atendam às condições de autorização no país.
A FDA declarou que este é o quinto teste autorizado que usa saliva como amostra. O teste de saliva elimina a necessidade de swabs nasofaríngeos, que também costumam apresentar escassez, e alivia o desconforto do paciente associado a esse tipo de coleta.
Uma vez que a amostra de saliva é autocoletada sob a observação de um profissional de saúde, ela também pode diminuir o risco para os profissionais responsáveis pelo recolhimento da amostra. A FDA observou um desempenho variável em testes com saliva. Por isso, determinou que o teste de Yale atende aos critérios para autorização de emergência para testar amostras de saliva para SARS-CoV-2.
Validação na prática
O método SalivaDirect está sendo validado como um teste para indivíduos assintomáticos por meio de um programa que testa jogadores e funcionários da NBA. Os resultados, até o momento, parecem ser precisos e semelhantes aos dos swabs nasofaríngeos para Covid-19 conforme os resultados de um artigo preprint publicado por Vogels e colaboradores no site medRxiv.
Segundo nota emitida por Yale, “o método SalivaDirect é mais simples, menos caro e menos invasivo do que o swab nasofaríngeo, método tradicional para detecção do SARS-CoV-2, e os resultados até agora revelaram que o SalivaDirect é altamente sensível e produz resultados semelhantes aos do swab nasofaríngeo.”
Fonte: PebMed|Autora: Roberta Esteves Viera de Castro.